Однофотонная эмиссионная компьютерная томография головного мозга в определении степени гипоперфузии
у пациентов с вертебробазилярной недостаточностью, вызванной позиционными нарушениями кровотока в задней черепной ямке
Состояние кровотока в головном мозге (ГМ) является предметом изучения для множества исследователей по всему миру. Сложность оценки перфузионных характеристик ГМ определяется широким диапазоном колебаний последнего в нормальных условиях и зависит от множества сопутствующих факторов. При патологии, определение нарушение перфузии становится ключевым для принятия решении об интервенции.
Критериев, определяющих критическое для ГМ снижение перфузионного кровотока не установлено. В отдельных работах предпринимаются попытки оценить параметры кровотока в норме у здоровых добровольцев, изучение же такового при патологии, это всегда вызов для исследователя. В прошлом, клинические решения относительно лечения сосудисто-нервных расстройств, приводящих к ишемии, определялись процентом стеноза рассматриваемого сосуда. Однако такой подход предполагает предсказуемую и стабильную взаимосвязь между процентом стеноза и степенью уменьшения кровотока, которую он вызывает. Исторически сложилось так, что этот тип отношений трудно было задокументировать. Таким образом, методы неинвазивного измерения абсолютного кровотока в конкретных церебральных артериях имеют потенциальную практическую ценность. Количество способов оценки кровотока с использованием современных технологии чуть более пяти. Среди них использование закиси азота [1], 133 ксенон (Xe) - однофотонная эмиссионная компьютерная томография (ОФЭКТ) [2], Xe- компьютерная томография (КТ) [3], позитронно-эмиссионная томография (ПЭТ) [4] динамический магнитно-резонансная томография (МРТ) [5], и перфузионная КТ [3]. Все они были использованы для измерения мозгового кровотока (МК) в различных клинических ситуациях. Существует как количественная, так и качественная оценка перфузии головного мозга. Качественная оценка предназначена для выявления изменений кровотока в каком-либо из сосудистых бассейнов у одного индивидуума при различных обстоятельствах, например при спровоцированной ишемии или при увеличении функциональной нагрузки на орган, приводящей к росту потребления кислорода.
Количественная оценка притока крови к мозгу может быть полезна для выявления пациентов с риском церебральной ишемии, вызванной нарушением гемодинамики. Гемодинамическая оценка с помощью количественной МР-ангиографии (qMRA) используется для выявления пациентов с высоким риском инсульта и важна для принятия решений о своевременном лечении [7]. qMRA позволяет определить общий мозговой кровоток, оценить влияние возраста и пола на МК, увидеть распределения МК в круге Уиллиса и помочь в анализе ауторегуляции кровотока в головном мозге, а также предположить различные цереброваскулярные нарушения [8].
Однако диапазон кровотока для отдельного здорового сосуда в головном мозге может быть весьма разнообразным из-за особенностей врожденной анатомии артерий и/или анатомических вариаций Уиллисова круга. Снижение кровотока в отдельном сосуде не обязательно может быть вызвано сосудистым заболеванием. Эффективная парадигма принятия решений, основанная на гемодинамической оценке, требует алгоритма, который учитывает как анатомические вариации, так и оценку потоков в дистальных сосудах (regional cerebral blood flow (rCBF)). Однако современные методы оценки rCBF технически сложны, требуют много времени и могут подвергать пациента воздействию длительного ионизирующего излучения. В большинстве исследований значения rCBF выражались в миллилитрах на 100 граммов ткани мозга в минуту без дифференцировки отделов или структур. Изредка, в работах по оценке МК можно натолкнуться на определение МК отдельно для белого и серого вещества. В исследовании Buijs P.C. с соавт. [4] о влиянии возраста на общий объем МК с использованием нерегулируемой односторонней двухмерная фазово-контрастной МР -ангиографии (2D PC MRA), был впервые предложен эмпирический коэффициент 10,81–12,14 для корреляции между общим МК (миллилитры в минуту), полученным при 2D PC MRA, и общим МК (миллилитров в минуту на 100 грамм ткани мозга) полученным при исследованиях с использованием закиси азота, 133Xe-SPECT, 99mТc-SPECT, Xe-КT и ПЭТ.
Достижения в различных радиоактивно меченных трассерах позволили картировать церебральную перфузию с качественным изображением. Первично, важен клинический интерес их использования в качестве меры оценки rCBF при патологических состояниях. 99mTc этилцистеинат димер (ECD) обладает высокой стабильностью in vitro и быстрым in vivo клиренсом; следовательно, его можно использовать для количественной оценки rCBF при соответствующем моделировании. Количественные подходы с 99mTc-ECD использовались на экспериментальных животных с индикаторной моделью фракционирования [9], а затем и на людях, используя постоянную потоковую константу [10]. Сообщалось о методах графического построения с использованием динамических планарных изображений или изображений ОФЭКТ. В нашем исследовании мы использовали простой неинвазивный метод для количественного определения rCBF с 99mTc ECD и ОФЭКТ на основе трехкамерной модели (рисунок 1). Для метода требуется один томограф и одноточечный доступ к венозной крови в оптимальное время после введения трассера.
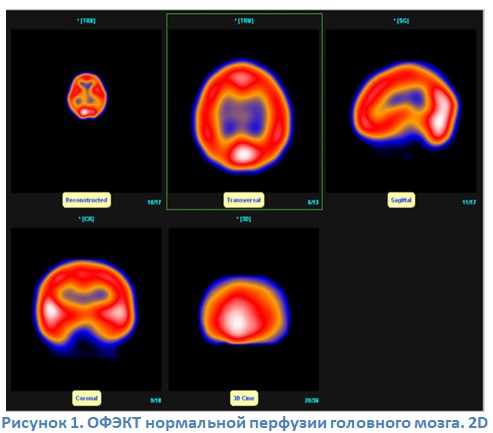
Используя ОФЭКТ у пациентов с вертебробазилярной недостаточностью (ВБН), по нашему мнению, может помочь объективизировать степень ишемии в соответствующих отделах головного мозга и установить показания к хирургическому вмешательству при декомпенсации кровообращения в задней черепной ямке. Недостаточность кровообращения в вертебробазилярном бассейне (ВББ) – это клинический симптомокомплекс, вызванный снижением перфузии ткани головного мозга в бассейне основной артерии (ОА). Этиологией вышеупомянутого патологического процесса служит уменьшение поступления крови по позвоночным артериям в заднюю черепную ямку. Компенсаторные механизмы Уиллисова круга успешно срабатывают при медленно протекающих окклюзионных процессах, как экстравазальных, так и интравазальных. Парадоксальность ситуации в том, что постепенно формирующаяся окклюзия позвоночной артерии (ПА), вызванная ли опухолевым процессом или атеросклеротической бляшкой – не вызывает симптомов ВБН. Более того, при окклюзии первого сегмента подключичной артерии с формированием Steal – синдрома по ПА, не наблюдается тяжелых клинических проявлений ВБН, и это несмотря на ретроградный кровоток по ПА, обеспечивающий кровоснабжение соответствующей верхней конечности [11]. Прерывистое же воздействие на позвоночную артерию различных структур (костная ткань, мембраны, элементы межпозвоночного диска) приводит либо к временному прекращению кровотока по ПА, либо к значительному снижению его объёма, и часто приводит к ярко выраженным симптомам ВБН [12,13]. При этом, не обязательно полная компрессия ПА в зоне контакта. Достаточно спровоцировать вазоспазм ПА, который рефлекторно распространяется на все ветви основной артерии, особенно заднюю соединительную артерию (ЗСА), приводя к функциональному размыканию Уилисова круга [14]. В результате мы имеем пациента, с позиционными “dropp” – атаками, без перспективы компенсации. Быстрое восстановление (нормализация) просвета ПА, возникающее после её спазма с последующим восстановлением кровообращения в ВББ не приводит к формированию коллатералей и/или неоангиогенезу, т.к. не запущены длительно протекающие молекулярные механизмы стимуляции роста сосудистого русла, как это бывает при хронических окклюзиях.
В связи с вышеизложенным, помощь пациентам с позиционными нарушениями кровотока в ВББ крайне затруднена. Трудности обусловлены как сложностями в диагностике, так и травматичностью инвазивного лечения экстравазальной компрессии ПА.
Целью настоящего исследования было определить степень снижения перфузии ткани ГМ при позиционной пробе Де Клейна, качественно оценив региональный мозговой поток, используя показатели, полученные с помощью ОФЭКТ.
Материалы и методы:
В исследование включено 114 пациентов с системными и несистемными головокружениями, обследованных в ГУ «Республиканский Научно-Практический Центр Неврологии и Нейрохирургии», 33-м из них определили показания к наружно-сонно-позвоночному перемещению в V3. Оперативные вмешательства проводились в ГУ «Республиканский научно-практический Центр Кардиология» (РНПЦК) и 4-ой городской клинической больнице г. Минска за период с 2003 по 2017 гг. Обследование и лечение проводилось в рамках научно-исследовательского проекта, финансированного комитетом по науке министерства здравоохранения Республики Беларусь и одобренного этическим комитетом РНПЦК. Средний возраст больных составил 48,1±0,8 лет (от 31 до 71 лет). Клинические и демографические характеристики пациентов с экстравазальной компрессией ПА во втором (V2) и третьем (V3) сегментах, представлены в таблице 1.
Таблица 1. Клинические и демографические характеристики, оперированных пациентов.
Характеристика | Показатель |
Возраст, лет | 48,1±0,8 |
Пол, мужчины n/(%) | 18 (54,5) |
Индекс массы тела, средний (кг/м2) | 23,5 ± 1,5 |
курильщики n/(%) | 3 (9) |
Сахарный диабет n/(%) | 2(6) |
Периферические вертеброгенные симптомы (%) | 100 |
Нистагм n (%) | 28 (84,8) |
Артериальная гипертензия n(%) | 6 (18,8) |
Посттравматическая энцефалопатия n(%) | 12 (36,6) |
Зрительные симптомы n(%) | 26 (78,8) |
Головные боли n(%) | 30 (90,1) |
Кохлеарные симптомы (%) | 100 |
Головокружение (%) (в том числе системное (%)) | 100 (37,7) |
Ромберга “+” проба де Клейна “+” (%) | 100 |
Синкопальные состояния, dropp – атаки (%) | 100 |
Астенические проявления n(%) | 17(51,5) |
Всем пациентам проводилось тестирование по шкалам Тиннети и оригинальной шкале (оВБН) для определения степени выраженности симптоматики. 13 пациентов были исключены из дальнейшего обследования в связи с легко степенной ВБН. У 18 пациентов выявлена умеренная степень ВБН (6-7 баллов по шкале оВБН, 11-20 баллов по шкале Тиннети); у 48 больных диагностирована выраженная ВБН (8-10 баллов (оВБН), 5 - 10 баллов по шкале Тиннети); грубые нарушения присутствовали у 35 пациентов (11-15 баллов (оВБН), менее 5 баллов по шкале Тиннети). Всем пациентам проводили ОФЭКТ с целью определения степени снижения перфузии ткани мозга в покое и при позиционной пробе Де Клейна. Пациенты были подразделены на группы по тяжести ВБН с целью выявления корреляционной связи клинических проявлений с результатами ОФЭКТ.
ОФЭКТ проводилась на двухдетекторном однофотонном эмиссионном томографе Nucline X-Ring/R («Siemens», Германия), в качестве РФП было применено 99mТс-ECD («Ceretec», Польша). Каждому больному РФП с активностью 555—740 МБк в 3—5 мл физраствора вводили в локтевую вену. Через 5 мин проводили ОФЭКТ. Каждое исследование включало 64 или 120 проекций мозга при матрице сбора проекций 64ґ64 или 128ґ128. Анализ срезов проводили в аксиальной, фронтальной и сагитальной проекциях с применением фильтра Low-Pass Cosine. Полученные томограммы оценивались визуально с определением зон или очагов сниженной радиоактивности, обусловленных снижением перфузии. В случае наличия таких очагов рассчитывался коэффициент асимметрии (КА), который вычислялся общепринятыми методами, по отношению радиоактивности в очагах ее снижения) к радиоактивности контралатерального участка.
Исследование выполнялось по однодневному протоколу в последовательности ОФЭКТ – «rest» головного мозга через 15 минут после введения РФП. Промежуток между исследованиями в покое и провокационной пробе Де Клейна составил в среднем 120 мин, что связано с необходимостью естественной элиминации препарата после предыдущего исследования. Второе исследование ОФЭКТ – «Stress» головного мозга с введением РФП через 5 минут после функциональной нагрузочной пробы Де Клейна, чтобы начало нарушения распределения Тх 99 приходилось на момент провокации динамического нарушения кровообращения. Пробу Де Клейна проводили только в сторону с наибольшим клиническим проявлением ВБН. Другие варианты поворота головы с её запрокидыванием могли бы привести к некорректным результатам, не позволяющим верифицировать этиопатогенез заболевания.
Результаты:
Состояние перфузии головного мозга в «покое» в группах пациентов представлено в таблице 2.
Таблица 2. Показатели ОФЭКТ головного мозга у пациентов с разностепенной ВБН в покое.
Зона оценки перфузии/ % п-в с гипоперфузией | умеренная ВБН 18 б-х | выраженная ВБН 48 б-х | грубые нарушения ВБН 35 б-х |
Лобная доля | 5,5 % | 10,4 % | 8,6 % |
Височно-теменная (справа+ слева) | 0 % | 0 % | 0 % |
Затылочная | 11 % | 10,4 % | 11,4 % |
Оценка показателей распределения изотопа у пациентов с ВБН сравнивалась с таковым у здоровых людей. Снижение плотности распределения изотопа в ткани мозга в состоянии покоя не превышала 10% от референтных показателей распределения препарата в группе здоровых пациентов. Поэтому, даже у тех пациентов, у которых мы наблюдали базовую гипоперфузию, она не была критической. В данном исследовании, мы ставили задачу выявить степень снижения накопления препарата при провокационной пробе Де Клейна. Оценка снижения его накопления от начального распределения препарата будет ключевой в определении ишемической этиологии симптоматики ВБН у обследованных нами пациентов.
Результаты влияния провокационной пробы Де Клейна на распределения изотопа в ГМ представлены в таблице 3.
Таблица 3. Показатели ОФЭКТ головного мозга у пациентов с разностепенной ВБН при пробе Де Клейна.
Зона оценки перфузии/ % п-в с гипоперфузией | умеренная ВБН (18 б-х) | выраженная ВБН (48 б-х) | грубые нарушения ВБН (35 б-х) |
Лобная доля | 44,4 % | 41,6 % | 42,8% |
Височно-теменная (справа+ слева) | 11,1 % | 6,25 % | 11,4% |
Затылочная | 55,5 %* | 62,5 %* | 85,7%* |
- - p< 0,05 по сравнению с показателями, выявленными в состоянии покоя.
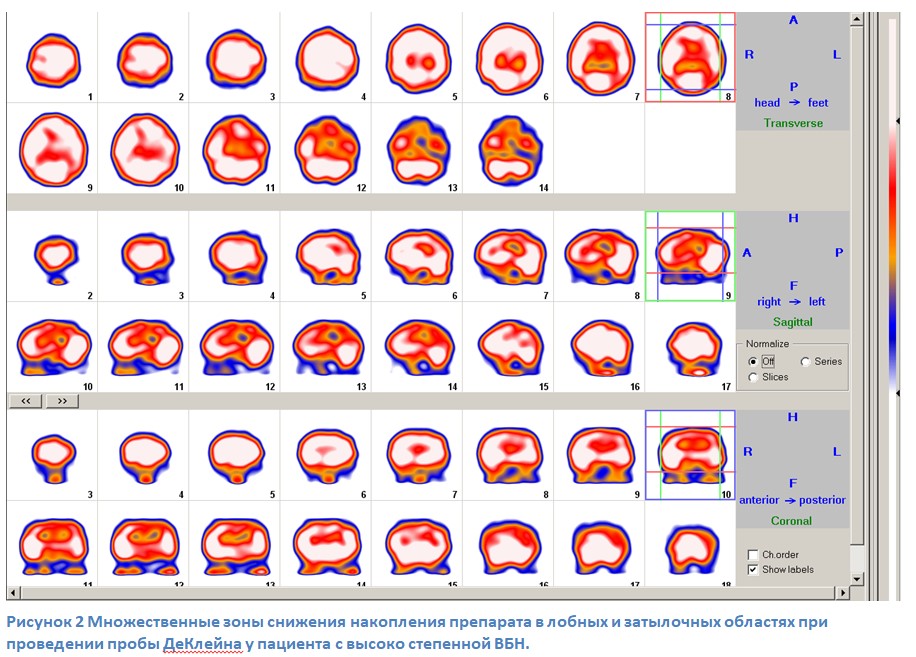
При провокационной пробе, зоны гипоперфузии ткани мозга логично усиливались в затылочной области, больше чем в 2 раза. При этом, обращает на себя внимание значительное увеличение зон гипоперфузии в лобных долях, что для нас было неожиданностью. Данный феномен касался только лобных отделов, т.к. в височно-теменных такого прироста мы не наблюдали (см. рисунок 2). Распределение в группах зон гипоперфузии более 20% от исходных показателей представлены в таблице 4.
Таблица 4. Количество пациентов со снижением показателей ОФЭКТ головного мозга более 20% при пробе Де Клейна.
Зона оценки перфузии/ % п-в с гипоперфузией > 20% | умеренная ВБН (18 б-х) | выраженная ВБН (48 б-х) | грубые нарушения ВБН (35 б-х) |
Лобная доля | 0 | 4,2% | 20% |
Височно-теменная (справа+ слева) | 0 | 0 | 2,8% |
Затылочная | 11,1% | 29,2% | 42,9%* |
- - p< 0,05 по сравнению с показателями, выявленными в состоянии покоя.
Прямая корреляционная связь между клиническими проявлениями ВБН и снижением перфузии на 20% и более при пробе ДеКлейна приблизилась к 1,0 (r=0,9) (рассчитывалась по показателям шкал Тиннети и оригинальной шкалы ВБН).
Обсуждение:
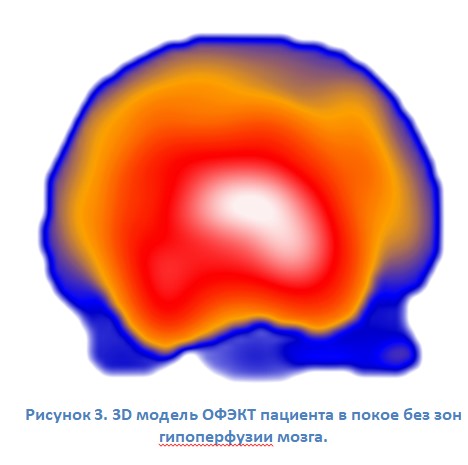
При оценке полученных данных ОФЭКТ, мы использовали как 2D так и 3D изображение для прецизионной оценки зон гипоперфузии. На рисунке 3 представлена 3D модель сцинтиграфии мозга (ОФЭКТ) в покое у пациента с позиционным нарушением мозгового кровообращения в задней черепной ямке. К сожалению, достаточно сложно представлять 3D картинку на плоскости и тем более делать по ней выводы о ценности исследования полученного в 3D. Тем не менее, для схематической демонстрации полученного результата этого вполне достаточно. На рисунке 4 представлена 3D картина того же пациента со снижением зоны накопления изотопа в задней черепной ямке более 20% после проведения провокационной пробы ДеКлейна.
Уникальность данного исследования в том, что определяя изменения перфузии головного мозга при провокации, мы исключаем другие механизмы, влияющие на накопление изотопа у данного конкретного пациента. Нам не нужно учитывать такие факторы, как наличие повреждения мозга в анамнезе, наличие гипертензии или гипотензии, избегать приема препаратов влияющих на мозговой кровоток. Более того, мы используем такого рода подход для определения эффективности определенного вида лечения ВБН, сравнивая показатели ОФЭКТ до начала приема препаратов и на фоне терапии или до операции и после. Изменения показателей накопления препарата относительно таковых в «покое» в один и тот же день, при тех же условиях, позволяет максимально объективизировать влияние примененного нами фактора на перфузию ткани мозга. Так, нами удалось выявить закономерность в появлении и/или усугублении гипоперфузии в затылочных отделах мозга при провокационной пробе ДеКлена. Благодаря достоверности полученных отличий (p<0,05) мы можем говорить о влиянии поворота головы с запрокидыванием ее назад (проба ДеКлейна) на изменение кровотока в задней черепной ямке. Поскольку данная проба является патогномоничной для определения степени воздействия экстравазального компонента на ПА, то мы с уверенностью можем утверждать, что причиной клинических проявлений ВБН у наших пациентов является патология во втором сегменте (V2) ПА.
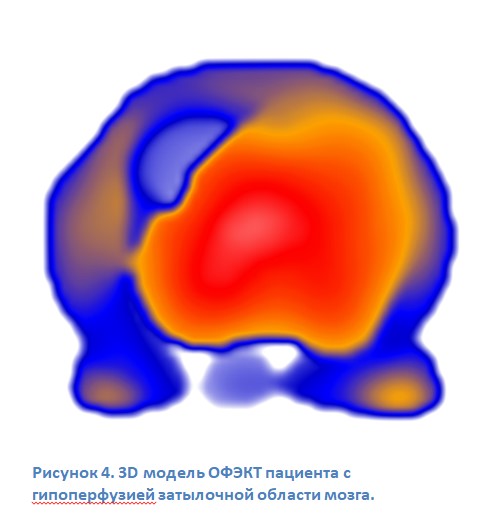
Уникальный факт, который был нами зафиксирован при проведении нагрузочной ОФЭКТ – это значимые снижения перфузии в зонах мозга, кровоснабжающихся из каротидного бассейна. Как видно из таблицы 1, у пациентов в состоянии покоя можно увидеть дефицит накопления препарата не только в затылочной области, что было бы вполне ожидаемо у больных с ВБН, но и в лобных доля. Данный феномен стал для нас довольно неожиданным, т.к. зона гипоперфузии в лобных и височно-теменных областях не могла зависеть от состояния кровотока по позвоночным артериям. Кроме того, нами выявлена прямая корреляционная связь снижения кровотока между затылочной и лобной областью при провокационной пробе Де Клейна (r=0,76) у пациентов с «грубыми нарушениями» ВБН. Оказалось, что уже в состоянии покоя мы видели нарушение накопления препарата лобных долях. После проведения пробы Де Клейна, гипоперфузия в задней черепной ямке усиливалась и сопровождалась таковой и в других отделах головного мозга, особенно в лобных долях. При этом корреляционная связь между пробой Де Клейна и снижением перфузии в лобных отделах имела прямую линейную зависимость. Объяснением данного феномена, может быть провокация поворотом головы спазма передних соединительных артерий, приводящего к снижению по ним кровотока и выпадением зон перфузии. Подтверждением данного предположения может служить факт пропадание сигнала («исчезновения») от передних соединительных артерий на транскраниальном доплере (ТКДГ) во время провокационных проб с дипиридамолом и Де Клейна. Поскольку всем пациентам в нашем исследовании проводилась ТКДГ, то сопоставление этих двух методов исследования позволило нам предположить рефлекторный механизм снижения перфузии ткани мозга в лобных отделах при провокации. Таким образом, можно говорить о наличии рефлекторной взаимосвязи, регулирующей интракраниальный кровоток. Эта взаимосвязь ранее в литературе не упоминалась, а значит данный процесс нуждается в дальнейшем изучении.
В последующем, было бы важно определить на сколько изменения кровотока в лобных долях могут приводить к клиническим проявлениям? Насколько они выражены у категории пациентов с ВБН? Не будут ли клинические проявления гипоперфузии в лобных долях (когнитивные нарушения) замаскированы клиникой вестибуллярных симптомов, как ведущей симптоматикой?
Выводы:
- ОФЭКТ головного мозга с провокационной пробой ДеКлейна может служить источником дополнительной информации о степени влиянии на перфузию ткани мозга экстравазальной компрессии позвоночной артерии во втором сегменте.
- Выполнение пробы Де Клейна на стороне поражения сопровождается значительным снижением перфузии в задней черепной ямке у пациентов с высокостепенной ВБН и имеет прямую корреляционную связь с тяжестью клинических проявлений ВБН (r=0,9).
- Впервые выявлены достоверные изменения перфузии ткани головного мозга на 20% и более в затылочной области по сравнению с состоянием «покоя» у пациентов с ВБН высокой степени (p<0,05).
- Снижение перфузии в лобных отделах, выявленная при ОФЭКТ с пробой ДеКлейна имеет прямую корреляционную зависимостью со степенью выраженности симптомов ВБН.
Литература:
- Fazekas JF, Alman R, Bessman AN. Cerebral physiology of the aged. Am J Med Sci 1952; 223:245–57.
- Ogasawara K, Ogawa A, Yoshimoto T. Cerebrovascular reactivity to acetazolamide and outcome in patients with symptomatic internal carotid or middle cerebral artery occlusion: a xenon-133 single-photon emission computed tomography study. Stroke 2002;33:1857–62.
- Wintermark M, Thiran JP, Maeder P, et al. Simultaneous measurement of regional cerebral blood flow by perfusion CT and stable xenon CT: a validation study. AJNR Am J Neuroradiol 2001;22:905–14.
- Kohki Oikawa 1, Masakazu Kobayashi, Takaaki Beppu, Kazunori Terasaki, Kuniaki Ogasawara Resolution of Hypoxic Tissue in Cerebellar Hemispheres After Arterial Bypass Surgery in a Patient With Symptomatic Bilateral Vertebral Artery Occlusion: A 18F-FRP170 PET Study. Clin Nucl Med. 2019 Apr;44(4):295-296.
- Carroll TJ, Teneggi V, Jobin M, et al. Absolute quantification of cerebral blood flow with magnetic resonance, reproducibility of the method, and comparison with H2(15)O positron emission tomography. J Cereb Blood Flow Metab 2002;22:1149 –56.
- Buijs PC, Krabbe-HartkampMJ, Bakker CJ, et al. Effect of age on cerebral blood flow: measurement with ungated two-dimensional phase-contrast MR angiography in 250 adults. Radiology 1998;209:667–74.
- Conway SA, Bowling SM, Geyer JD, Potts DC, Clemons BL, Gomez CR. Quantitative magnetic resonance angiography of the cerebrovasculature in physiologic and pathologic states. J Neuroimaging. 2008 Jan;18(1):34-7.
- Zhao, S. Amin-Hanjani, S. Ruland, A.P. Curcio, L. Ostergren and F.T. Charbel Regional Cerebral Blood Flow Using Quantitative MR Angiography American Journal of Neuroradiology September 2007, 28 (8) 1470-1473;
- Greenberg JH, Araki N, Karp A. Correlation between 99mTc-bicisateand regional CBF measured with iodo-[14C]antipyrine in a primate focal isehemia model. J Cereb BloodFlow Metab. 1994;14(suppl 1):S36-S43
- Pupi A, Castagnoli A, Teresa RM, Cristofaro D. Bacciottini L, Petti AR. Quantitative comparison between 99mTc-HMPAO and 99mTc-ECD: measurement of arterial input and brain retention. EurJNuclMed 1994;21:124-130.
- Osiro S, Zurada A, Gielecki J, Shoja MM, Tubbs RS, Loukas M. A review of subclavian steal syndrome with clinical correlation. Med Sci Monit. 2012 May;18(5):RA57-63.
- Soustiel JF, Bruk B, Shik B, Hadani M, Feinsod M. Transcranial Doppler in vertebrobasilar vasospasm after subarachnoid hemorrhage. Neurosurgery. 1998 Aug;43(2):282-91
- Yancy H, Lee-Iannotti JK, Schwedt TJ, Dodick DW. Reversible cerebral vasoconstriction syndrome. Headache. 2013 Mar;53(3):570-6.
- Yancy H, Lee-Iannotti JK, Schwedt TJ, Dodick DW. Reversible cerebral vasoconstriction syndrome. Headache. 2013 Mar;53(3):570-6.
Терехов В.И.






